Novità: le Simulazioni del test di Medicina 2024, interamente commentate e sulla Banca Dati.
Tutti i quiz sono commentati passo passo. Stessa composizione del test ufficiale, stesso tempo a disposizione (100 minuti), stesse logiche di attribuzione del punteggio e tutte le simulazioni hanno graduatoria nazionale. Acquistale da qui >
Nelle ultime due edizioni del test, i bilanciamenti delle redox hanno sempre avuto un quesito a loro dedicato, quindi investiamo senza indugio il nostro tempo e aggiudichiamoci questo succulento punto e mezzo!
Le ossidoriduzioni (o redox) sono un tipo di reazione chimica, in cui almeno una coppia di atomi cambia il proprio numero di ossidazione. Questo è dovuto al passaggio di elettroni da un atto ad un altro. In particolare uno dei due atomi cede elettroni, ossidandosi, mentre l’altro, che li acquista, si riduce.
Numero di ossidazione?
Il numero di ossidazione è definito come la carica che un atomo avrebbe se gli elementi di legame (quindi gli elettroni a comune) fossero assegnati all’elemento più elettronegativi e coincide con la carica dell’elemento quando è in forma monoatomica.
Fissati ora questi concetti, vediamo come si bilancia una reazione redox risolvendo un quesito, in particolare prenderemo il quiz numero 46 del test di medicina 2019:
Quale delle seguenti combinazioni di coefficienti stechiometrici – a, b, c, d, e – deve essere utilizzata per bilanciare la reazione
aCu + bHNO3 → cCu(NO3)2 + dNO + eH2O ?
Da dove partire nei quiz con le ossidoriduzioni.
La prima cosa da fare è assegnare i numeri di ossidazione ad ogni atomo della reazione, così da stabilire quale sia la specie che si ossida e quella che si riduce. Un elemento può avere più numeri di ossidazioni diversi, quindi come assegnare quello corretto?
La prima regola da tenere presente è che, in un composto, la somma algebrica dei numeri di ossidazione degli elementi che lo compongono è uguale a 0 o alla carica del composto, qualora presente.
Tutti i n.o. sono seganti sulla tavola periodica ma, dato che al test non la potrete portare, è bene ricordarne alcuni:
Il fluoro ha sempre n.o.= -1
L’ossigeno ha n.o.= -2 (fuorché in una particolare specie chimica, i perossidi, dove ha n.o. = -1)
L’idrogeno ha n.o.= +1 (tranne che negli idruri dove invece ha n.o.= -1)
I metalli alcalini (primo gruppo) hanno n.o.= +1
I metalli alcalino terrosi (secondo gruppo) hanno n.o.= +2
Gli elementi puri hanno n.o.= 0
Applichiamo queste regole all’esempio
Cu0 + H+1 N+5 O3-6 → Cu+2 (N+5O3-6) + dN+2O-2 + H2O
_______
🏅Dispensa consigliata: Equilibrio chimico e Costante di equilibrio: Dispensa per i test Medico-Sanitari. Clicca qui per leggere >
_______
In questo caso abbiamo quindi che l’azoto, acquisisce 3 elettroni riducendo il n.o. da 5 a 2, mentre il rame di ossida, cedendo 2 elettroni. Tuttavia noi sappiamo che gli elettroni che l’azoto acquista sono gli stessi che il rame cede, quindi dovranno essere 6 (3*2) sia per il Cu che per l’N. Per cui il primo passo per bilanciare la reazione è equilibrare gli elettroni, facendo in modo che le specie si scambino 6 elettroni.
3Cu + 2HNO3 → 3Cu(NO3)2 + 2NO + H2O
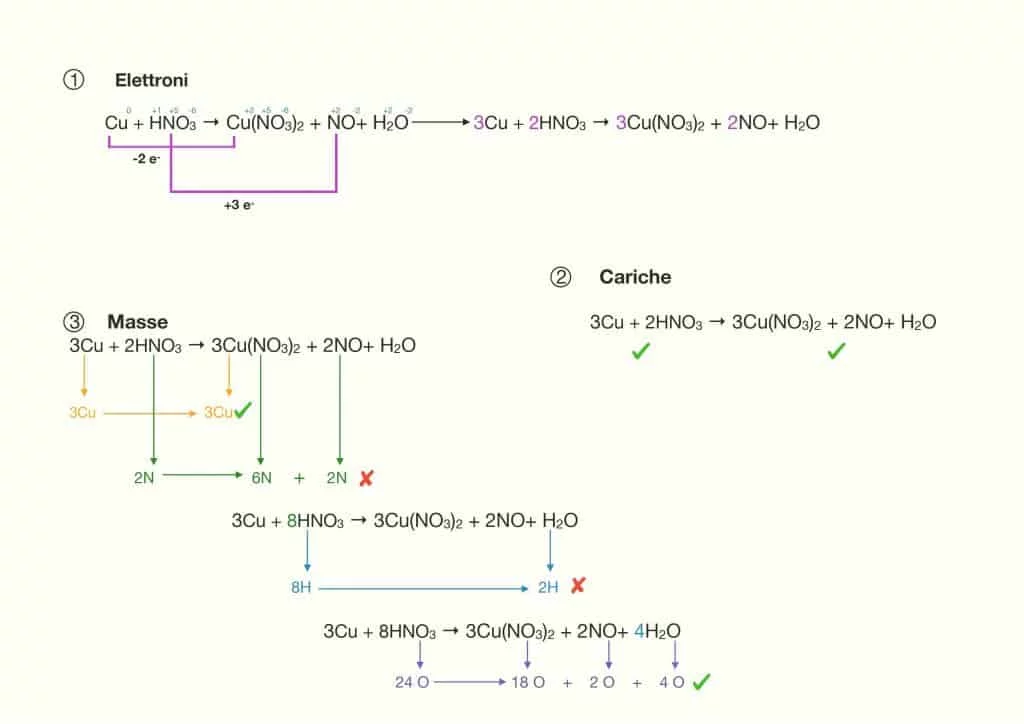
Il passaggio successivo è quello di equilibrare le cariche, ovvero assicurarsi che la carica assoluta della reazione sia la stessa da un lato o dall’altro dell’equazione, bilanciando un’eventuale squilibrio con l’aggiunta di una specie ionica. Dato che nell’esempio specifico non ci sono ioni, le cariche della reazione sono già bilanciate. Questa fase ai fini del test è trascurabile.
Passiamo quindi all’ultimo step: equilibrare le masse. Ogni specie reattiva deve essere rappresentata in ugual misura sia da un lato che dall’altro dell’equazione (per il principio di conservazione di massa) e per farlo, si studiano i singoli elementi.
Consiglio pratico: Lasciate ossigeno ed idrogeno per ultimi.
Il rame è già in equilibrio, con tre atomi a destra e tre a sinistra. L’azoto invece è sbilanciato, con 2 atomi a destra e 8 a sinistra, per cui aggiungiamo 6 al coefficiente stechiometrico minore. In questo momento la reazione è scritta come:
3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO + H2O
Passando agli idrogeni, questi sono 8 a sinistra e 2 a destra, quindi dovremo bilanciarli. Dato che a sinistra gli idrogeni sono 2 in ogni molecola d’acqua, bisognerà aggiungere la metà del coefficiente (in questo caso 3) a quello già presente, ovvero 1 (implicito).
3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO + 4H2O
Studiando infine gli ossigeni, questi sono 24 atomi sia a destra che a sinistra. La reazione è bilanciata!
_______
🏅Dispensa consigliata: Come calcolare la resa di una reazione in 7 passaggi. Clicca qui per leggere >
_______
I passaggi da mettere in pratica nei quiz con le ossidoriduzioni sono quindi:
1 Bilanciare gli elettroni.
2 Bilanciare le cariche, se necessario.
3 Bilanciare le masse.
Ossidoriduzioni: reazioni di dismutazione
Vediamo adesso un caso particolare di redox, svolgendo il quesito numero 45 del test di medicina 2018:
Quali sono i valori da attribuire ai coefficienti a, b, c per bilanciare correttamente la seguente reazione chimica?
3Cl2 + aNaOH → bNaClO3 + cNaCl + 3H2O
Punto 1: assegnamo i n.o. e bilanciamo gli elettroni:
3Cl20 + aNa+1O-2H+1 → bNa+1Cl+5O3-6 + cNa+1Cl-1 + 3H2O
Si noti come, in questo caso, il cloro in parte si riduca nel formare un composto e in parte si ossidi nel formarne un altro. Questo tipo di reazioni sono chiamate dismutazioni, ma restano comunque reazioni di ossidoriduzione. Quindi procediamo come sappiamo.
Il Cl in un caso perde 5 elettroni per formare NaClO3, mentre ne acquista 1 per formare NaCl, quindi assegno 5 come coefficiente al cloruro di sodio.
3Cl2 + NaOH → NaClO3 + 5NaCl + 3H2O
_______
🏅Dispensa consigliata: Il reagente limitante: come individuarlo velocemente in una reazione. Clicca qui per leggere >
_______
Anche qui le cariche sono bilanciate, quindi procediamo con le masse.
Il cloro è già bilanciato, al contrario del sodio, che ha 5 atomi a sinistra più che a destra. Andando quindi a sommare, scriverò a sinistra 6 come coefficiente dell’idrossido di sodio:
3Cl2 + 6NaOH → NaClO3 + 5NaCl + 3H2O
Guardando idrogeni ed ossigeni, vediamo che la reazione è già bilanciata così.
Ecco la nostra ricetta per non temere mai più le ossidoriduzioni.
Speriamo davvero questa dispensa ti sia piaciuta, se vuoi continuare a studiare alla grande puoi seguirci su Instagram (seguici su @promed_official) e/o entrare nei nostri percorsi di preparazione avanzati.
Alla prossima
Pro-Med Family










